泉州MDRCE认证的费用-需要什么材料
更新时间:2025-03-01 浏览数:394
所属行业:
咨询 管理咨询
发货地址:上海市浦东新区陆家嘴街道
产品数量:9999.00个
价格:面议
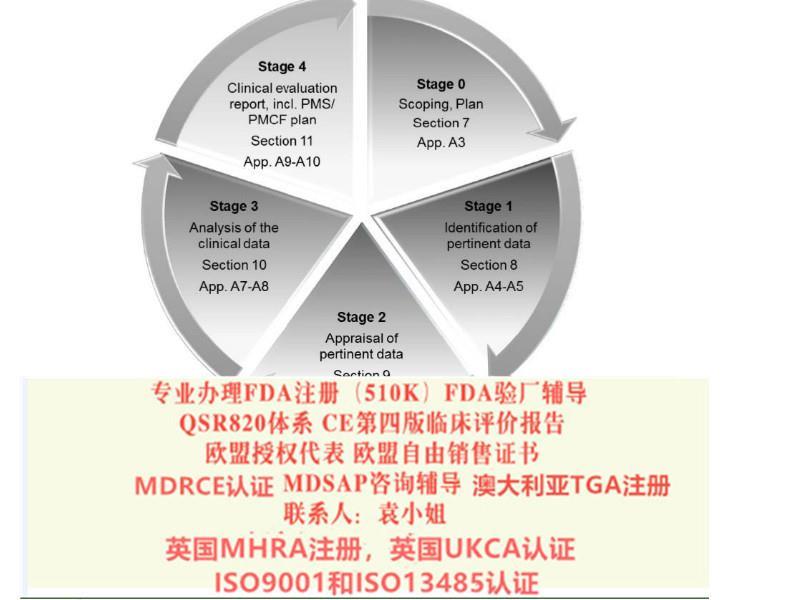
2019 年5 月25 日,MDR 正式生效, 替代了原医疗器械指令(MDD,93/42/EEC)和主动植入式医疗器械指令(AIMD,90/385/EEC)。
2019 年4 月5 日,欧洲议会和理事会正式签发了欧盟关于医疗器械2019/745 号法规(MDR,EU2019/745),5月5日,欧盟官方期刊(Official Journal of the EuropeanUnion) 正式发布该法规
仅具有根据90/385/EEC 和93/42/EEC 指令签发的证书的器械可投放市场的前提是自MDR 适用之日起,其在设计和预期目的上无显著变化并符合新法规有关市场后监察、市场监察、警戒、经济运营商及器械注册的规定。
医疗器械法规(MDR)转换期为3年,2020年5月4日起强制实行。体外诊断器械法规(IVDR)转换期为5年,2022年5月4日起强制实行。
2016年12月14日,EUDAMED(European databank for medical devices) 筹划指导**上欧盟各国对于医疗器械法规MDR及IVDR的执行进行了一轮的讨论,与会人员对于这两个法规的细节内容进行了讨论并达成了一致意见。在此基础上,会议对于MDR及IVDR的执行达成了如下时间表。
MDR 由指令升级为法规,提高了对欧盟成员国的约束力,具有直接约束性,*各国转化为本国的法律法规的形式即可落实实施

MDR 在整合原指令的基础上,大幅提升了有关医疗器械认证的规范和限制,例如关于产品分类规则、器械的可追溯性、临床性能研究的规范、增加上市后的产品*性和有效性的监管等方面。MDR 共10 章123 条,并附有17 个附录。
总的说来新的MDR和IVDR加强了体系管理,对高风险设备增加了相关规定比如对于非医疗用途但具有与医疗器械相似特性的设备也将受到新法规的管辖(如用于美容的彩色隐形眼镜),提升了产品对患者的透明度和可追溯性并设立*电子数据库(Eudamed)、医疗设备将有一个一的识别号这加强其在整个供应链的可追溯性。
MDR 在很多方面的规定都趋于加严格的监管模式,加强调持续监管和*协作的监管方式。
MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来,与一般医疗器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断医疗器械指令98/79/EEC。
-/gbaaeee/-
http://sungoyuan.b2b168.com