服务专业讲解
优势执行力高
价格合理优惠
特点量身定制
周期短
项目ce-mdr
地区全国
标准一站式全包服务
售后服务包售后
评价
◇产品测试报告及相关文献
◇使用概述及观点
附1、产品出厂检测报告
附2、产品型式检测报告
附3、基本要求检查表
备注:
◇研究(包括:物理性能,生化、药理 、药动及毒性研究,测试,灭菌合格,药物相容性等)
◇生物兼容性测试(A)部分要求:细胞毒性、感光性、-皮内反应、急性全身中毒、致热性、亚急性中毒、遗传毒性、植入溶血性; (B)支持测试:慢性中毒、致癌性、再生性/生长性、生物动因退化。)
◇资料(需要研究或描述研究)
◇包装合格
◇标签、使用说明
◇结论(设计档案资料的接受、利益对应风险的陈述)
10、欧盟授权代表信息及协议
11、符合基本要求表
12、协调标准
13、警戒系统程序

MDRCE认证
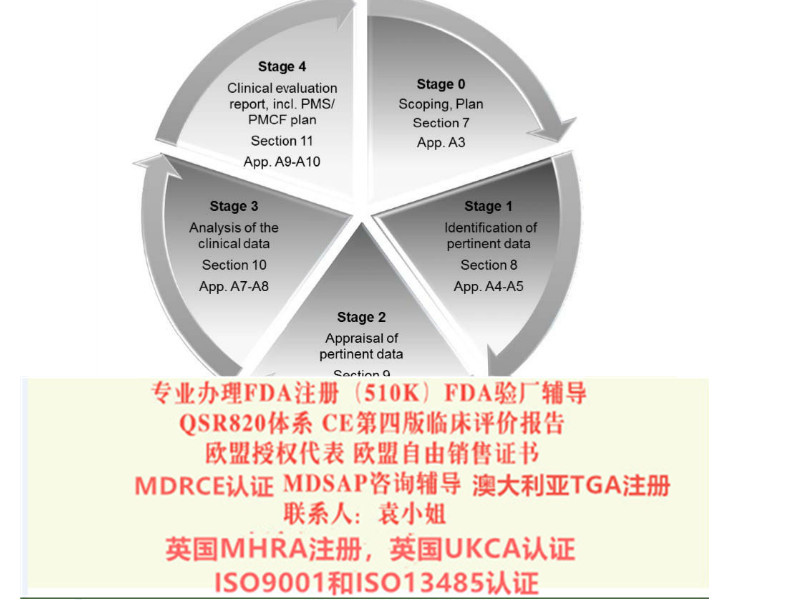
按照Medical Device Regulation 2017/745/EU法规 做CE技术文件
我公司可以帮助您整理并建立高质量的CE技术文件
评估产品和已有技术文件的情况,识别存在的差距;
确认产品应符合的标准,并制造商安排相关的测试、确认;
根据制造商的具体情况,沟通并完成风险管理报告;
评估制造商的资料,编写评价报告;
编写CE技术文件或设计文档;
若需要,可以提供后续的法规更新服务。
Medical Device Regulation 2017/745/EU法规是什么?
SUNGO集团凭借**网络和队伍为**客户提供法规,帮助企业*贸易壁垒,在器械行业尤为专长。
这主要包括:欧盟CE认证(MDD/MDR)、欧盟授权代表、器械欧盟注册、欧盟自由销售证书、FDA注册(FDA510K)、FDA验厂,陪审和翻译、ISO9001/ISO13485,中国局注册证、GMP体系和生产许可证等项目。

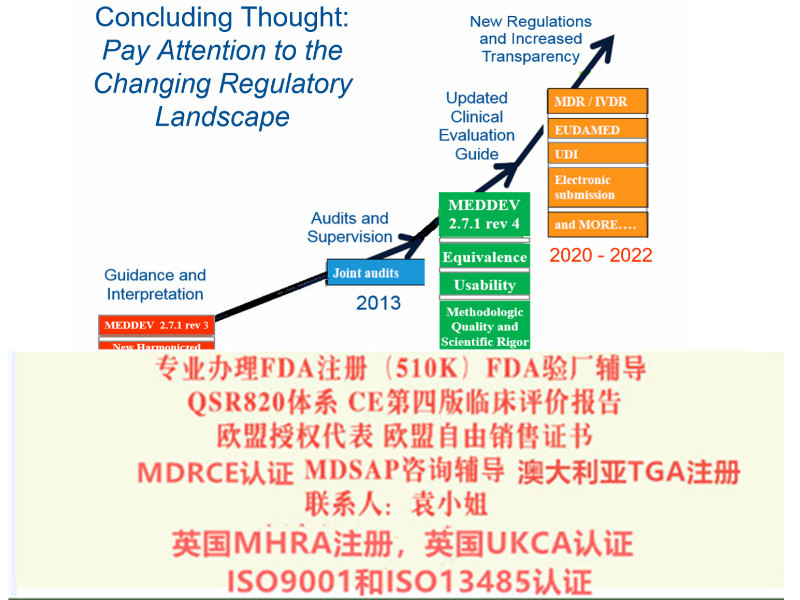
关于欧盟CE 认证的MDR法规升级:
老指令MDD 93/42/EEC including 2007/47/EC 升级到新法规MDR EU 2017/745
2017年5月,欧盟器械新法规MDR (REGULATION EU 2017/745) 颁布,新的法规将替代原有的器械指令 (MDD 93/42/EEC) 和有源植入性器械指令 (AIMDD 90/385/EEC) 。
从2020年5月开始公告机构不能按照MDD颁发CE证书,目前I及以上风险等级产品认证机构已不再受理MDD指令的认证申请。
对于目前获得CE证书的企业,应基于自身设备的证据的充分性合理安排申请MDR的时间,尽快启动MDR法规合规准备事宜
欧盟会规定了MDR 的转换期的要求
2017 年5 月25 日:MDR 和IVDR 生效
2020 年3 月25 日:启动欧盟器械数据库(Eudamed)
2020 年5 月25 日:MDR 实施开始
2022 年5 月25 日:IVDR 实施开始
2024 年5 月25 日:AIMD,MDD 和IVDD 证书将失效

什么是合格评定?
产品在投放市场之前要进行合格性评估
需要满足所有立法要求
包括测试,检查和认证
适用产品法规中规定了每种产品的程序
合格评定的目的:
为了投放市场的产品符合所有法规要求
该程序应确保消费者,公共当局和制造商对产品的一致性充满信心
http://sungoyuan.b2b168.com