品牌SUNGO
欧代荷兰
周期4周
有效期5年
流程SUNGO
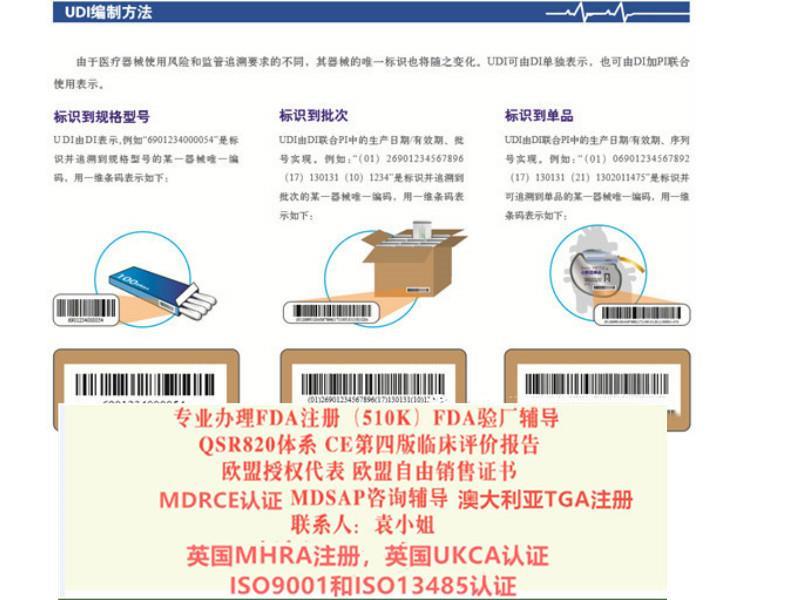
法规条款增加,认证评审更加严格, 引入了器械标识UDI,增加产品的可追溯性;
2012年,欧盟会起草了MDR和IVDR法规,当中历时了4年的时间,直到2016年6月,欧洲议会和欧盟理事会才发布MDR和IVDR的文本。

我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE*四版评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系、食品FDA验厂及整改、OTC药品FDA验厂及整改
中国法规:器械产品备案登记表、器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证、SFDA验厂、SFDA注册检测、企业标准编制、局自由销售证。
出口其余国际法规:器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂、ISO22716 GMPC验厂、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
MDR范围的变化
MDR纳入更多产品进行管理;
• MDR中附录XIV所列的非用途的产品:
• 眼镜;
• 用于修改或固定身体部位的植入物;
• 面部或其他皮肤或粘膜填充剂;
• 设备;
• 用于人体的有创激光设备;
• 强脉冲光设备
MDR分类规则的主要变化
• 仍为4类: Class I, IIa, IIb, III
• Duration of Use (无变化)
-Transient < 60 minutes;
- 60minutes < Short-term<30 days;
- Long term > 30 days
• 18 个规则=> 22个规则
- Rule 1-4 Non invasive devices
- Rule 5-8 Invasive devices
- Rule 9-12 Active devices
- Rule 13-22 Special rules
分类规则: 1-4 Non invasive devices
Rule 3:
• 在原来基础上, 新增由一种或几种物质混合组成的非侵入器械,其预期用于直接在体外接触已从人体或人体胚胎中取出且还未被植入人体的细胞、组织或,该类器械属于III类。
分类规则: 5-8 Invasive devices
Rule 6、 7:
• 在原来基础上, 新增用于直接接触心脏或循环系统的短暂、短期使用型侵入性手术器械属于III类

市场监督,警报,经济运营和设备登记的规定。可通过免税订单获得,符合新规定的设备可在2020年5月26日前投放市场。符合新规定的合格评定机构可在2020年5月26日前并通知。可以采用合规合规评估程序,并在2020年5月26日之前根据新规定颁发证书。
我司注意到新法规主要在以下几点上发生了变化:1.器械的定义;2.器械的分类;3.基本和性能要求;4.技术文件要求;5.评价;6.上市后;7.Eudamed数据库;8.对NB公告机构的要求(新法规生效后NB将按照新的要求重新进行授权);9.对高风险器械的新增了要求;2017年2月器械法规(MDR)和体外诊断器械法规(IVDR)终提案发布,2017年3月7日欧盟28个成员国一致表决同意欧盟采用新版的器械法规(MDR)和体外诊断器械法规(IVDR)。
我公司申请:出口瑞士:需要瑞士代表,瑞士注册
http://sungoyuan.b2b168.com









