品牌SUNGO
欧代荷兰/德国
周期4周
有效期5年
注册CIBG注册
我们为企业编写的MDR CE技术文件里的:风险分析报告,评价报告,基本基本检查表等等,不仅仅是为了获得一张证书而做的,更多的都是从各个方面来产品是的有效的。
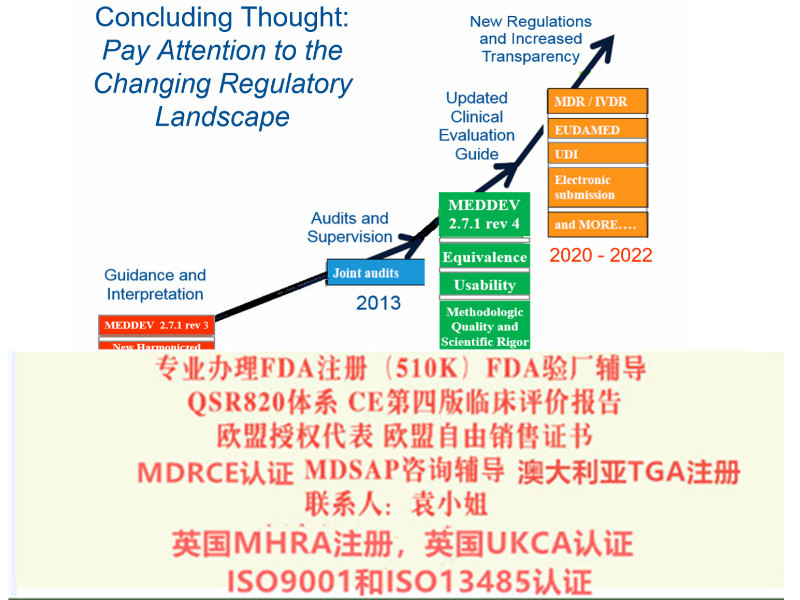
法规条款增加,认证评审更加严格
法规条款增加,认证评审更加严格,分类规则增加:由MDD的18条增加到 22条;
这里还存在一个端情况,打比方,公告机构在2020年5月25号,也是MDR强制实施的前版发了一张MDD CE证书,这张证书有效吗?能管几年的时间? 这张证书的有效期不是5年了,而是4年,有效期到2024年5月27号。看下以下这张表格可以说是一目了然的,虽然2020年05月26号MDR强制实施,并不意味着2020年05月26号之后,按照原93/42/EEC指令颁布的MDD证书失效,但是所有按照原93/42/EEC指令颁布的MDD证书将会于2024年05月27日失效,所以2024年05月27日是一个截止日期。

合格评定根据某些装置的危险类别和具体特征,对符合CE标志的装置的评价各不相同(*五十二条)。所有IIa、IIb和III类设备以及一些特定的I类设备都需要一个通知机构的干预(见*7a5、b6和c7段)。*52条和附件九、十、习叙述了根据设备类别不同的评估方法。在某些情况下,制造商对合格评定路线有一些选择。对于某些III类和IIb类设备,有一个新的评估咨询程序,该程序将由一个立的组根据该公告机构的评估评估报告进行(*五十四条)。附件一规定了一般的和性能要求,附件二和三规定了技术文件的组成。质量管理体系的范围(*10条*9款)包括评价和上市后随访。评价计划必须先于评价本身(附件十四,A部分)。

我司注意到新法规主要在以下几点上发生了变化:1.器械的定义;2.器械的分类;3.基本和性能要求;4.技术文件要求;5.评价;6.上市后;7.Eudamed数据库;8.对NB公告机构的要求(新法规生效后NB将按照新的要求重新进行授权);9.对高风险器械的新增了要求;MDR&IVDR修订要点15) 欧盟代表与进口商和制造商一起起到连带责任欧盟代表要求, 类似于法规负责人16) 平行贸 Parallel Trade, 特别是重新贴标签或重新包装17) 一次性器械的再加工和使用:- 符合成员国的法规要求- 再加工方要承担法定制造商的责任;- 由机构或外部加工方进行的一次性MD的再加工和再使用必须要符合通用技术规范或协调标准或成员国的法规要求.- 再加工器械的和性能应等同于初期的一次性MD18) 植入器械: 患者应获得基本的信息, 包括标识, 危害健康的警示或注意事项19) 带有CE标记的MD, 在欧盟内可以自由流通和销售. 但成员国可以限制某些器械的使用.20) 除了定制器械外, 所有器械都应应用UDI系统 (MDR执行后1-5年)21) EUDAMed, MD的 命名Code22) 植入和III类产品的制造商应公开产品的主要和性能, 及评估结果的概要.- 和性能的概要应特别包括该产品在与其他诊断或方法比较时的重要性,和二者的使用条件23) 在欧盟的层面上管理NB
关于MDR涵盖产品范围和分类规则:器械的分类继续以前的类别,根据风险等级分为四类:I,II a,II b,III。但是,分类规则从18增加到22.具体分类规则的条件和变化如下:关于经济运营商的义务:该法规在章*2条的定义中提出了“经济运营者”的概念。
瑞士也已经不认可欧洲的CE认证,您有产品出口瑞士吗?是否有做瑞士代表以及瑞士注册的?
http://sungoyuan.b2b168.com









