服务专业讲解
优势执行力高
价格合理优惠
特点量身定制
周期短
项目ce-mdr
地区全国
标准一站式全包服务
售后服务包售后
作为器械制造商(生产商)产品在欧盟市场销售,需要做哪些工作呢?
制造商应做的事情:
在将产品投放市场之前准备技术文档
确保技术文档提供给市场当局(应要求看到它)只要产品投放市场
自产品投放市场之日起,将技术文档保存10年(除非另有明确规定)

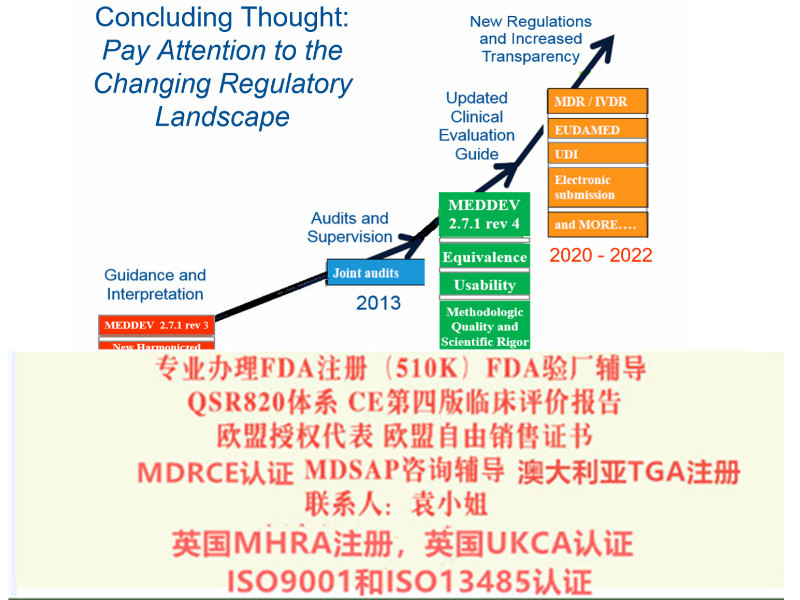
欧盟会规定了MDR 的转换期的要求
2017年5 月25 日:MDR 和IVDR 生效
2020年3 月25 日:启动欧盟器械数据库(Eudamed)
2020年5 月25 日:MDR 实施开始
2022年5 月25 日:IVDR 实施开始
2024年5 月25 日:AIMD,MDD 和IVDD 证书将失效
我们该怎么办?
l 重新确认产品风险分类等级,确认是否有风险等级升级的情况?
例如部分可重复使用的器械,原属于ClassⅠ的器械,按照新法规变成了ClassⅠ类器械。美容类产品原MDD下不属于范围,现MDR法规中已纳入;
l 确认原CE证书的发证机构是否已获得欧盟当局批准的颁发MDR证书的资质,目前拥有该资质的认证机构:BSI、TUV南德(注意TUV莱茵目前还未获得批准);
l 确认原CE认证时的技术文件中是否含有按照Rev4原则提供的评价报告;
l 确定企业合规负责人(MDR法规要求),有相应能力、资质和经验来承担相应的法规工作职责。
l 修改原CE技术文件,建立质量管理体系,向具有MDR发证资质的认证机构提出MDR-CE认证申请,获得MDR法规下的新CE证书。

Q:证书未在过渡期结束前签发怎么办?
A:对于持有符合MDD或AIMDD的CE证书的制造商,将有3年的过渡期来满足MDR的要求。
在过渡期按照MDD和AIMDD签发的CE证书,在正式生效日期(2020年5月26日)后将继续有效,但有效期多不能**过4年。而在过渡期结束后的证书有效性取决于法规Article 120 clause 3所述规定。
如果您符合MDD的CE证书在过渡期内失效,且又未在过渡期内取得符合MDR的CE证书。那么你的产品必须从欧盟市场退出,直到产品获得符合MDR的CE证书才可重新上市。
Q:公告机构何时开始按照MDR进行符合性评审?
A:所有公告机构需要获得欧盟主管当局的认可后,才能按照MDR进行审核。
什么是合格评定?
产品在投放市场之前要进行合格性评估
需要满足所有立法要求
包括测试,检查和认证
适用产品法规中规定了每种产品的程序
合格评定的目的:
为了投放市场的产品符合所有法规要求
该程序应确保消费者,公共当局和制造商对产品的一致性充满信心
http://sungoyuan.b2b168.com









