PVC手套欧盟MDR证书怎么申请 ce医疗器械认证mdr 评估包含什么
更新时间:2025-08-29 浏览数:44
所属行业:
咨询 管理咨询
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
服务欧盟授权代表
代申请欧盟注册
申请CE认证
编写CE技术文件
建立ISO13485
IVDR
IVD产品如果想进入欧盟市场,需要CE认证
欧盟会(EC)的DG SANTE部门(健康和食品总局)负责这件事情
但各成员国的具体的落实需要靠CA(器械部门),由NB(备案机构)按照欧盟指令和法规要求执行器械产品的符合性评估和认证
执行的标准开始是按照90年代出的器械法规中的IVDD来IVD,但是由于这个标准太松,2017年正式上了新法规IVDR,2022年取代IVDD
原来按照IVDD标准批的证书2024年将过期
也是现在还处于过渡期
新的法规更加关注:产品、性能评估、评价、上市后
产品分类也有了变化:class ABCD
classA的要求可能,产家自我声明即可
class BCD都需要NB
通过了CE认证的产品可以在36个流通,一些东南亚也认可
在此日期之后,将不再有效的AIMDD / MDD证书。是否可以在2024年5月27日之前同时获得有效的MDR和AIMDD / MDD证书?是。在过渡期结束后,制造商是否仍然可以投放市场/投入使用符合指令的设备?是的,在某些条件下,可以选择继续投放市场/投入使用符合指令的设备,直到其现有证书到期为止。 这可以避免在MDR下立即需要新证书。要使用此选项,所有现有证书必须有效(例如,QMS),设备的目的和性质不得更改,并且您必须遵循新的MDR规则进行注册,监视和警惕。(EU)2017/745是指CE认证新的法规MDR,之前是MDD指令93/42/EEC现在CE认证由MDD指令升级到MDR法规了,所以整体要求都提高了很多。打个比方:之前考试60分可以及格,现在要80分才能及格;之前考试考三门,现在考试考五门。所以整个难度提升很多。
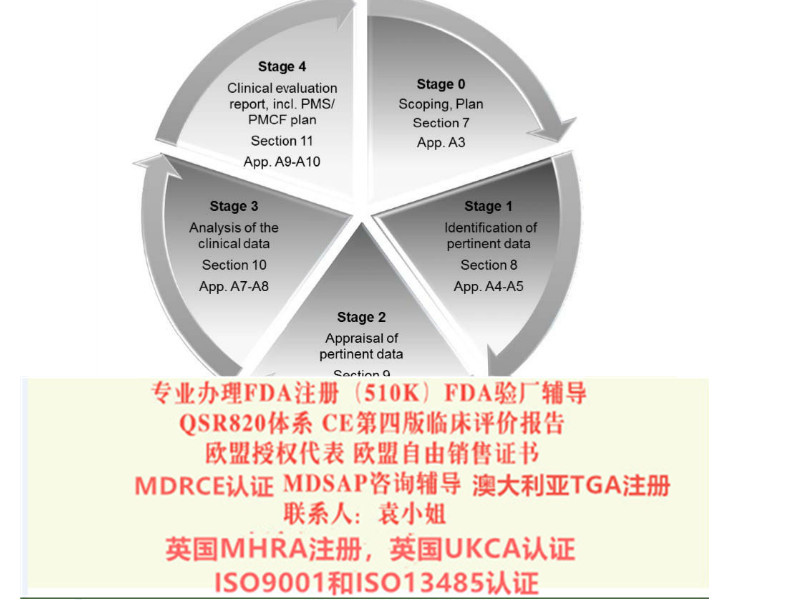
2017年5月5日,欧盟(Official Journal of the European Union)正式发布了欧盟器械法规(REGULATION (EU) 2017/745,简称“MDR”)。

MDR于2017年5月发布,标志着MDD和AIMDD之间为期三年的过渡期的开始。在过渡期间,MDR将逐步生效,先是与公告机构和制造商根据MDR申请新证书的能力有关的规定。过渡期将于2020年5月26日,即MDR法规的“适用日期”(DoA)结束。从那时起,MDR将完全适用。

MDR将有源器械指令(现行的90/385/EEC)纳入了进来,与一般器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断器械指令98/79/EEC。
我公司申请: 出口英国需要UKCA认证,英国代表,MHRA注册
http://sungoyuan.b2b168.com









