拐杖EU2017/745认证 mdr认证医疗器械
更新时间:2025-08-29 浏览数:24
所属行业:
咨询 管理咨询
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
周期4周
费用SUNGO
品牌SUNGO
欧代荷兰
注册CIBG注册
现有MDD客户重大变更的申请期。虽然MDR的正式实施有延期,但是有例外情况如:
· MDD产品的投放截止日期仍为2024年5月26日
· MDD产品供应截止日期仍为2025年5月26日。
公告机构何时开始按照MDR进行符合性评审?
MDR法规 共10 章123 条,并附有17 个附录。

Medical Device Regulation 编写MDRCE认证技术文件的流程

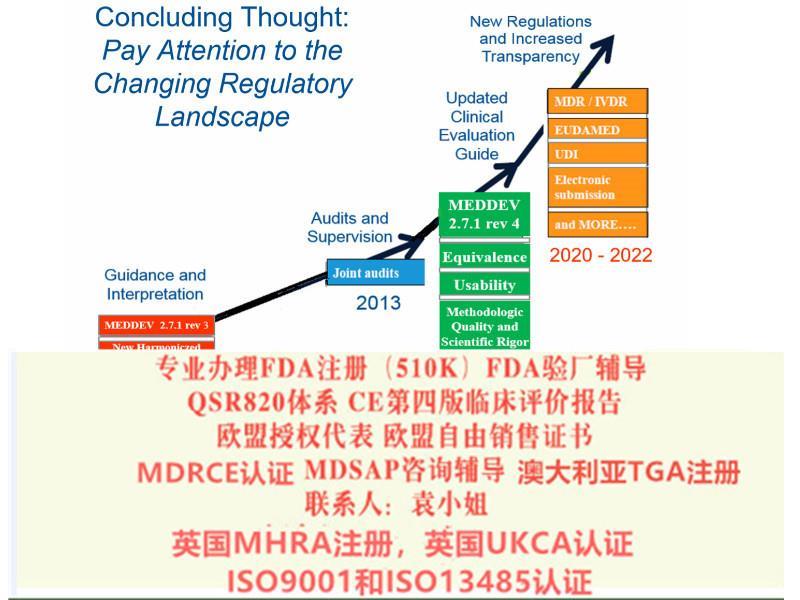
申请欧盟CE认证(CE整套技术文件编订、 CE*四版评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书
欧盟普通器械条例MDR法规EU 2019/745详解(上)
B 设计和制造相关的要求
• 10)化学、物理和生物特性
SUNGO是**化的器械法规技术服务商。从事行业服务达13年,累计服务客户**过4000家。在美国FDA注册、欧洲注册以及中低风险器械的认证业务上,市场份额长期稳居行业位,得到客户普遍**。选择SUNGO,不是选择了一次性的合作伙伴,而是选择了一个长期的技术支持的战略伙伴。
http://sungoyuan.b2b168.com









