PVC手套2017/745认证 EN ISO11199 MDR 2017/745号法规附
更新时间:2025-08-30 浏览数:29
所属行业:
咨询 管理咨询
发货地址:上海市金山区
产品数量:9999.00个
价格:面议
品牌SUNGO
欧代荷兰
周期4周
注册CIBG
有效期5年
欧盟授权代表保存制造商的技术文件,供主管部门检查。
新的器械法规(2017/745 / EU)(MDR)和体外诊断器械法规(2017/746 / EU)(IVDR)使欧盟立法与技术进步,科学变革和进步在法律制定上保持一致。
新法规将建立一个健全,透明,可持续的框架,得到国际认可,可提高*性并为制造商创造公平的市场准入。与指令不同,法规不需要转变为国家法。
器械法规(MDR)的背景
MDR将取代现有的器械指令(93/42/EEC)(MDD)和主动植入式器械指令(90/385/EEC) (AIMDD)。MDR于2017年5月发布,标志着MDD和AIMDD之间为期三年的过渡期的开始。
在过渡期间,MDR将逐步生效,首先是与公告机构和制造商根据MDR申请新证书的能力有关的规定。
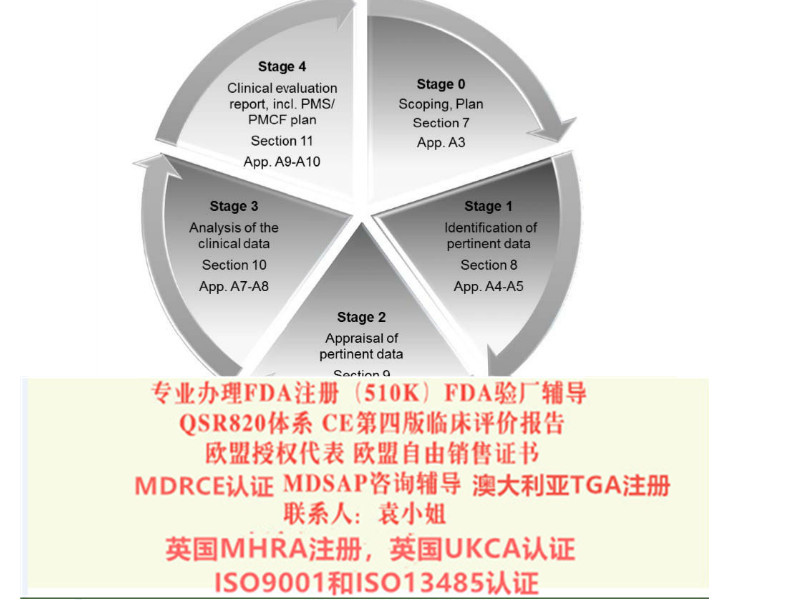
合格评定根据某些装置的危险类别和具体特征,对符合CE标志的装置的评价各不相同(*五十二条)。所有IIa、IIb和III类设备以及一些特定的I类设备都需要一个通知机构的干预(见*7a5、b6和c7段)。*52条和附件九、十、习叙述了根据设备类别不同的评估方法。在某些情况下,制造商对合格评定路线有一些选择。对于某些III类和IIb类设备,有一个新的评估咨询程序,该程序将由一个立的组根据该公告机构的评估评估报告进行(*五十四条)。附件一规定了一般的和性能要求,附件二和三规定了技术文件的组成。质量管理体系的范围(*10条*9款)包括评价和上市后随访。评价计划必须先于评价本身(附件十四,A部分)。

可以为某些设备制定确定附加要求的通用规范(*9条)。器械法规(MDR)何时适用MDR(EU)2017/745将于2020年5月26日起申请 - “申请日期”(DoA)。MDR的某些条款将提前生效(例如关于公告机构和器械协调组)。 有些将在稍后申请(例如关于UDI标签)。

在产品上市之前即明确了上市后制造商的责任和义务,并使得上市后有相应的依据。其次是持续的理念,关于评估,法规规定:公告机构应至少每隔12 月开展一次适当的审核和评估,以确保相关制造商采用批准的质量管理体系和上市后计划,公告机构至少应每隔五年随机对制造商进行一次现场突击审核。包括对制造商经营场所的审核,必要时还包括对制造商的供应商和/ 或分包商的审核。
SUNGO依靠这些资源,我们为**的器械生产商和经营者提品全生命周期的市场准入服务。
http://sungoyuan.b2b168.com









