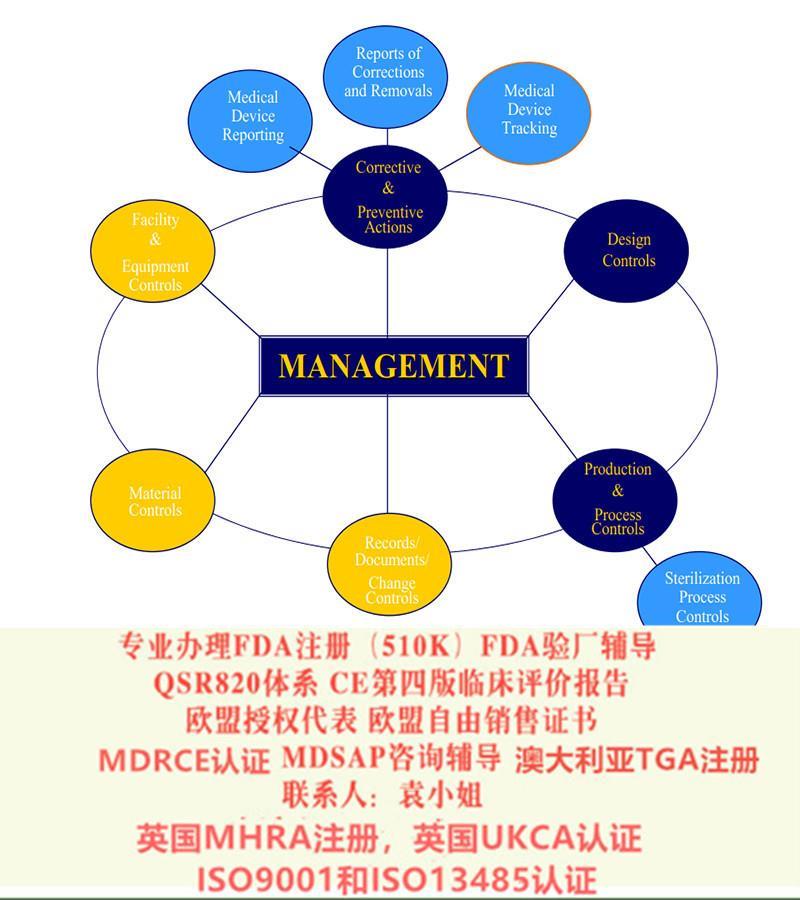
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
美国代理人
美国法规规定,所有境外的企业有医疗器械和食品进口到美国都需要位于美国境内的代理人,协助其在美国境内与官方机构和客户进行联络和协调。
SUNGO能够为您提供美国代理人服务,对于与美国境内公司及官方机构沟通有丰富的经验
美国FDA医疗器械企业注册和FDA医疗器械产品列名
按照FDA的规定,境外的医疗器械企业需要进行注册才能够将产品出口到美国。企业注册(Facility Registration)需要由美国代理人完成,且每年都需要进行年度新,下一年度注册信息新的时间区间为当年的10月1日到12月31日
按照FDA的规定,境外的医疗器械企业除了进行企业注册之外,还需要进行产品列名(Device Listing)。部分器械不需要510K或者PMA的可以直接进行列名。企业注册和列名完成之后会在FDA的上显示
每年10月1日到12月31日之间新企业的注册信息,否则注册将会失效。
美国FDA规定,在2016年10月1日到12月31日期间进行2019年度再注册,如果到12月31日之前未能按期注册,2019年FDA的注册和认证将会失效。因此,为确保贵公司的FDA注册在2019年继续有效,请贵公司尽快安排续费。

FDA会不定期随机地与美国代理人联系,对于信息不真实的代理人否则,会进行处罚,甚至注销工厂的注册编号

美国代理人代表国外工厂,FDA将视美国代理人的陈述为国外工厂的陈述

-/gbaaeee/-
http://sungoyuan.b2b168.com