我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
MDR&IVDR法规的变化(3)
4. 细化注册要求
General Safety and Performance Requirements
CE技术文件的要求
DOC的要求
NB的授权要求
Implant Card for implanted device
5. 加强市场监管要求
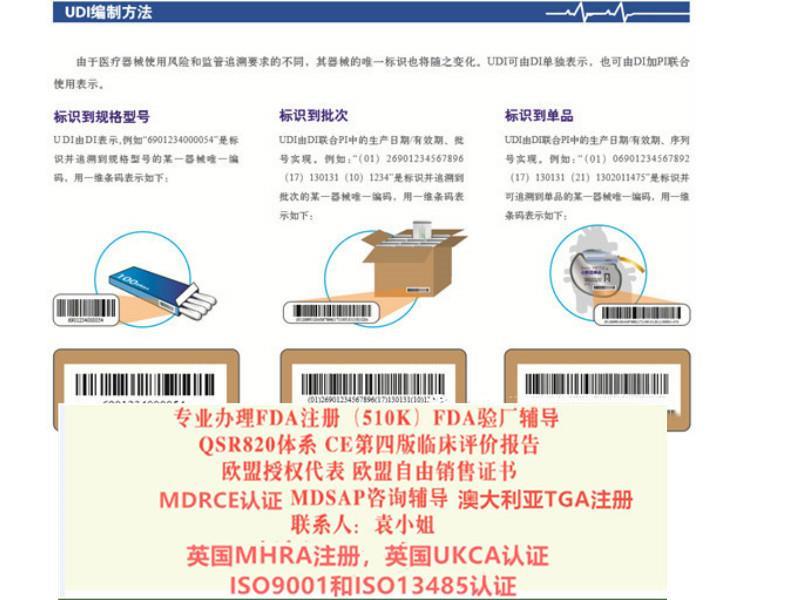
UDI要求
Eudamed数据库
加强欧盟成员国之间的监管协作
NB应满足的要求-Annex VII
• MDR对NB的要求加严格
• NB的授权和监管由多个国家主管当局联合组成的审核小组进行审核;
• NB必须要有自己的审核*团队,新法规下对外聘*的做法将有所限制;
• NB必须要有自己的临床*,而不能仅靠外部临床*进行相关审核。
• 新法规生效后, NB将按照新的资质要求重新授权,不符合要求的NB将会被淘汰。
• 对于已经CE证的企业,应密切关注其NB的新授权以及授权范围!!
与高风险MD有关的新要求
• 对于III类植入器械和用于注入和/或移除药物的IIb类有源器械,其临床评价报告,除了NB审核以外,还需要由NB交至主管当局进行expertpanel review,综合意见进行审评。
• 对于III类和植入器械(顾客定制除外) , 制造商应提交Summary of safety and clinical performance至NB。经NB审核后上传至EUDA MED数据库,供公众查询。
The manufacturer shall mention
on the label or instruc- tions for
use where the summary is available .(Article 32)
• 植入器械- Implant Card
(Article 17)
我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
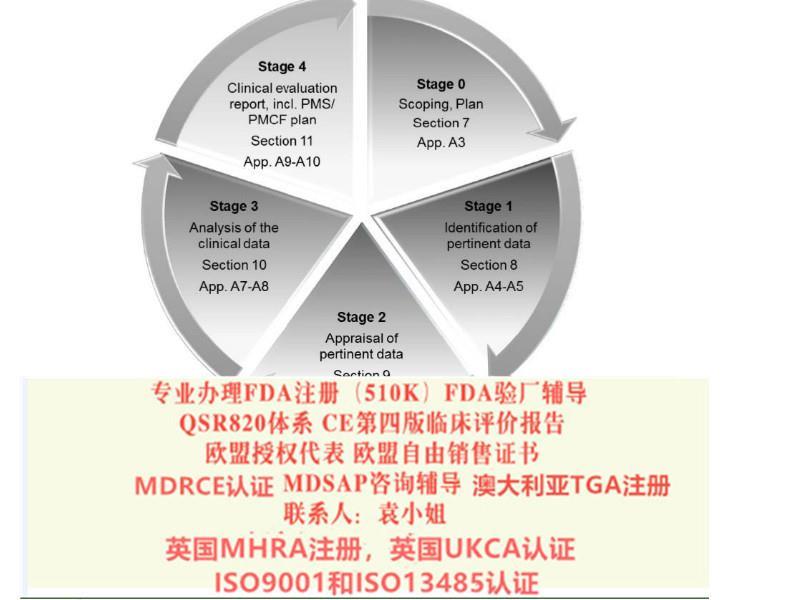
2019年2月医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)较终提案发布,2019年3月7日欧盟28个成员国一致投票表决同意欧盟采用新版的医疗器械法规(MDR)和体外诊断器械法规(IVDR)。2019年5月5日,欧盟正式发布了OfficialJournal其正式对外宣布了新版MDR(REGULATIONEU2019/745)法规和新的IVDR(REGULATIONEU2019/746)法规。新法规将取代现行的三个医疗器械指令:分别是医疗器械指令93/42/EEC,有源医疗器械指令90/385/EEC及体外诊断医疗器械指令98/79/EEC。

我们可以为您提供的自主服务项目主要有:
出口欧洲法规:欧盟CE认证(CE整套技术文件编订、 CE四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016认证、欧盟授权代表(德国,英国和荷兰)、欧盟注册、欧盟自由销售证书、防护服PPE指令Type5/6认证
出口美国法规:医疗器械、化妆品、食品美国FDA注册(含FDA510K申请)、美国代理人、 FDA 验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL、QSR820体系辅导、食品FDA验厂辅导及整改、OTC药品FDA验厂辅导及整改
中国法规:医疗器械产品备案登记表、医疗器械产品注册证、生产备案登记表、生产许可证、经营许可证、ISO9001/13485认证辅导、SFDA验厂辅导、SFDA注册检测、企业标准编制、药监局自由销售证。
出口其余法规:医疗器械单一体系审核MDSAP认证、澳大利亚TGA注册、BSCI验厂辅导、ISO22716 GMPC验厂辅导、BRC 认证,口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试
欧盟代表的法律责任
所有在欧盟境外的企业,必须以书面形式,授权在欧盟境内的个人或法人作为其授权代表,处理和MDR&IVDR相关的法律事宜。
- 对于制造商对欧盟代表的书面授权,只有欧盟代表书面确认后,该授权才生效,一种器械只能有一个欧盟代表;
- 当主管当局提出,欧盟代表应将授权书提供给主管当局;
- 欧盟代表至少应负责确认制造商已经建立CE技术文件、签发符合性声明、履行了符合性评估流程、履行了注册责任。应保存有制造商的CE技术文件、符合性声明、CE证书,并在需要时提供给主管当局;
- 应负责及时在主管当局和制造商之间传递信息,协助采取纠正预防措施;
- 应及时将投诉、事故等信息传递给制造商;
- 如果制造商不履行法律责任,欧盟代表对缺陷产品承担连带赔偿责任;
- 如果制造商不履行法律责任,欧盟代表有权终止委托,并立即报告主管当局;
-当制造商变欧盟代表时,制造商、新欧盟代表、原欧盟代表应签署三方协议,约定职责交接日期、资料交接、后续投诉/事故信息转达等事宜;
- 应至少任命一名负责法规合规性的员工,应有4年以上医疗器械法规事务或质量管理体系工作经验,或理工科、药学、医学大学以上*加1年医疗器械法规事务或质量管理体系的工作经验
进口商、经销商的法律责任
进口商:
应确认生产商已欧盟代表、已签发符合性声明、已使用UDI、标签说明书符合要求、已正确使用CE标志;
- 器械或其包装或其随机文件上,应注明进口商名称、注册地址、联系地址和注册商标等信息;
- 应确认器械已在欧盟数据库注册登记,进口商自身也应登记获得SRN;
- 应确保器械在符合生产商要求的环境里存储和运输;
- 应对客户投诉、召回、不合格品记录在案,并通知生产商及欧盟代表;
-/gbaaeee/-
http://sungoyuan.b2b168.com









