在DoA之后,现有指令下的公告机构颁发的证书是否仍然有效?
是的,AIMDD / MDD证书通常在的到期日之前有效。 这适用于通知机构通常颁发的所有证书,包括EC设计检验证书,合格证书,EC型式检验证书,EC证书*质量保证体系和EC证书生产质量保证。
但是,所有在2017年5月25日之后签发的证书迟在2024年5月27日之前无效。在此日期之后,将不再有效的AIMDD / MDD证书。
是否可以在2024年5月27日之前同时获得有效的MDR和AIMDD / MDD证书?
是。
在过渡期结束后,制造商是否仍然可以投放市场/投入使用符合指令的设备?
是的,在某些条件下,可以选择继续投放市场/投入使用符合指令的设备,直到其现有证书到期为止。 这可以避免在MDR下立即需要新证书。
要使用此选项,所有现有证书必须有效(例如,QMS),设备的目的和性质不得改,并且您必须遵循新的MDR规则进行注册,监视和警惕。

2017年5月5日,欧盟期刊(Official Journal of the European Union)正式发布了欧盟医疗器械法规(REGULATION (EU) 2017/745,简称“MDR”)。MDR将取代Directives 90/385/EEC (有源植入类医疗器械指令)and 93/42/EEC(医疗器械指令)。依据MDR Article 123的要求,MDR于2017年5月26日正式生效,并与2020年5月26日期正式取代MDD(93/42/EEC)和AIMDD(90/385/EEC)。日前公告机构BSI获得了欧盟新法规MDR(EU 2017/745)的资格授权。也意味着近期BSI、TUV南德、TUV莱茵、***等公告机构,也陆续可以开始受理MDR的申请。
MDR实施之后,在三年过渡期内仍然可以按照MDD和AIMDD申请CE证并保持证的有效性。依据Article 120 clause2 的规定,过渡期内NB签发的CE证继续有效,但是从其交付日期起有效期不**过5年,并且于2024年5月27日失效。
MDR的主要变化
1.扩大了应用范围
2.提出了新的概念和器械的定义
3.细化了医疗器械的分类
4.完善了器械的通用*和性能要求
5.加强对技术文件的要求
6.加强器械上市后的监管
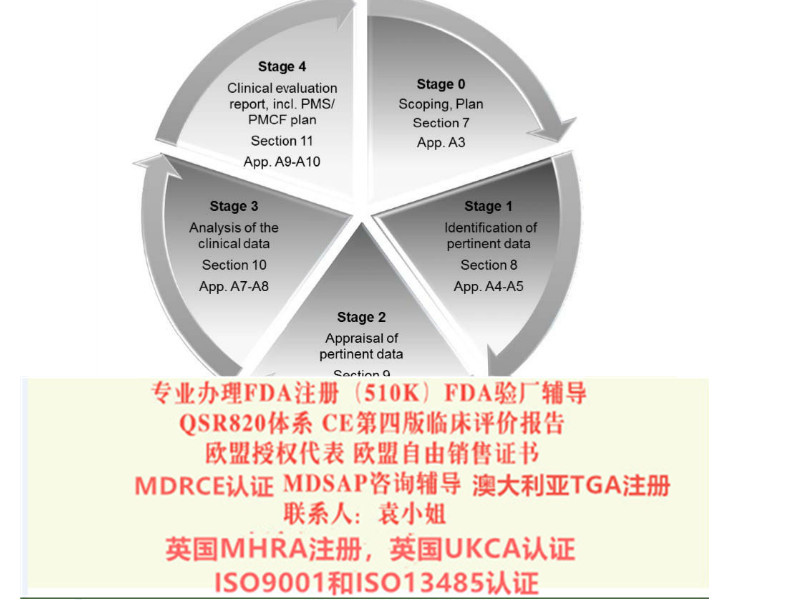
7.完善临床评价相关要求
8.提出Eudamed数据库的建立和使用
9.提出器械的可追溯性(UDI)
10.对NB提出严格的要求
医疗器械法规(MDR)何时适用
MDR(EU)2017/745将于2020年5月26日起申请 - “申请日期”(DoA)。
MDR的某些条款将提前生效(例如关于公告机构和医疗器械协调组)。 有些将在稍后申请(例如关于UDI标签)。
现有指令什么时候停止适用?
一般而言,指令90/385 / EEC和93/42 / EEC将于2020年5月26日(DoA)废除。
设备和制造商都必须遵守MDR。 您应该评估设备的符合性 - 这可能需要公告机构的参与。
其他重点包括:
•临床评估
• 风险管理
•质量管理体系(QMS)
•上市后监督
•技术文档和其他报告
•有缺陷设备的责任。

注意到新法规主要在以下几点上发生了变化:
1.医疗器械的定义;
2.医疗器械的分类;
3.基本*和性能要求;
4.技术文件要求;
5.临床评价;
6.上市后监管;
7.Eudamed数据库;
8.对NB公告机构的监管要求(新法规生效后NB将按照新的要求重新进行授权);
9.对高风险医疗器械的新增了要求;
总的说来新的MDR和IVDR加强了体系管理,对高风险设备增加了相关规定比如对于非医疗用途但具有与医疗器械相似特性的设备也将受到新法规的管辖(如用于美容的彩色隐形眼镜),提升了产品对患者的透明度和可追溯性并设立电子数据库(Eudamed)、医疗设备将有一个的识别号这加强其在整个供应链的可追溯性。
提醒我们的客户在申请医疗产品CE认证时,在过渡阶段请谨慎考虑是选用法规还是采用老的指令方案,同时也需要对NB机构的发证资格进行了解和确认以保证产品在欧盟市场销售的可延续性。
办理出口:美国FDA注册(含FDA510K申请)、 FDA QSR820验厂辅导及整改、FDA警告信应对&RED LIST REMOVAL/QSR820体系辅导/OTC验厂辅导及整改、CE认证(CE整套技术文件编订、 CE四版临床评价(MEDDEV 2.7.1 Rev 4)编写)、ISO13485:2016、欧盟授权代表、欧盟自由销售证书、英国BRC认证咨询,BSCI验厂辅导;口罩NELNSON(尼尔森)检测:(EN 14683检测、BFE检测,VFE检测、PFE检测)、手术衣EN13795测试、防护服type5/6 (PPE认证咨询(89/686/EC个人防护指令辅导)。
2017年2月医疗器械法规(MDR)和体外诊断医疗器械法规(IVDR)终提案发布,2017年3月7日欧盟28个成员国一致投票表决同意欧盟采用新版的医疗器械法规(MDR)和体外诊断器械法规(IVDR)。2017年5月5日,欧盟正式发布了OfficialJournal其正式对外宣布了新版MDR(REGULATIONEU2017/745)法规和新的IVDR(REGULATIONEU2017/746)法规。新法规将取代现行的三个医疗器械指令:分别是医疗器械指令93/42/EEC,有源医疗器械指令90/385/EEC及体外诊断医疗器械指令98/79/EEC。
2017年5月5日欧盟发布OfficialJournal
在这里需要特别说明的是欧盟此次是直接发布的Regulation(法规)而相比较之前的Directive(指令)其区别在于:提高了文件的约束力,发布立即在欧盟成员国生效并成为有约束力的法律,此次的Regulation*向Directive那样需要经过成员国转化成当地法律法规去落实实施。
医疗器械法规(MDR)转换期为3年,2020年5月4日起强制实行。体外诊断器械法规(IVDR)转换期为5年,2022年5月4日起强制实行。MDR将有源医疗器械指令(现行的90/385/EEC)纳入了进来,与一般医疗器械指令(现行93/42/EEC)合二为一,IVDR直接取代了现行的体外诊断医疗器械指令98/79/EEC。
-/gbaaeee/-
http://sungoyuan.b2b168.com









