CEMDR认证-CEMDR认证和MDRCE认证的区别

做莱茵的CEMDR证书要多少钱?什么是CEMDR?

Medical Device Regulation 2017/745/EU法规是什么?
SUNGO集团凭借**网络和队伍为**客户提供法规性服务,帮助企业*贸易壁垒,在医疗器械行业尤为专长。
这主要包括:欧盟CE认证(MDD/MDR)、欧盟授权代表、医疗器械欧盟注册、欧盟自由销售证书、FDA注册(FDA510K)、FDA验厂辅导,陪审和翻译、ISO9001/ISO13485,中国药监局注册证、GMP体系辅导和生产许可证等项目。
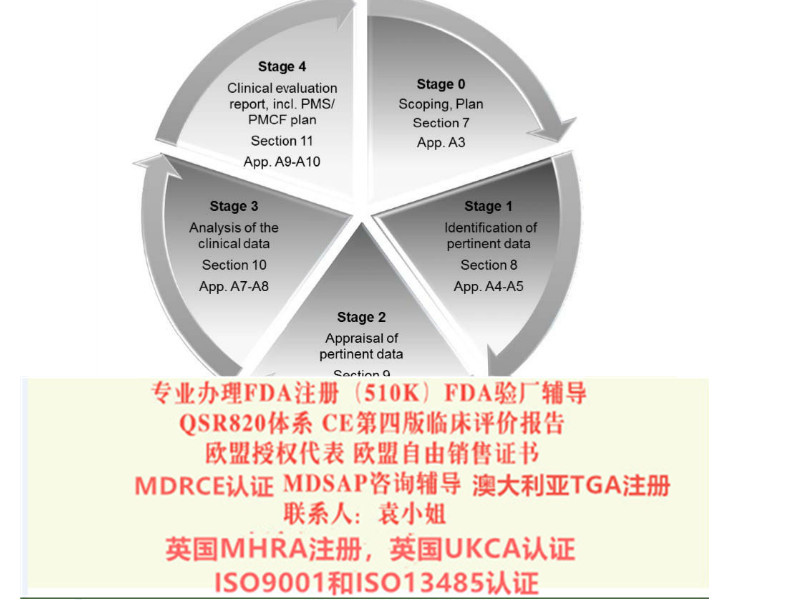
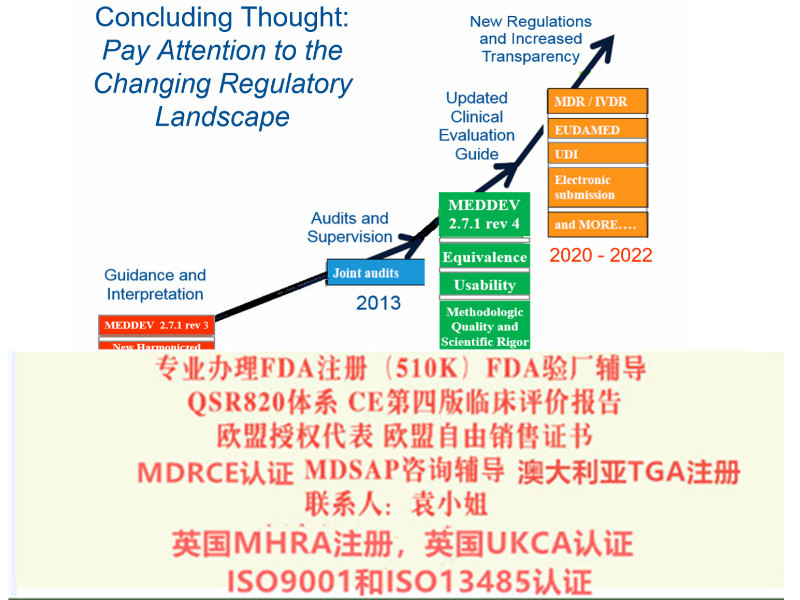
CE四版临床评价报告MEDDEV 2.7/1 Rev. 4
近两年,欧盟加强了临床评价和上市后监督的要求。2016年7月,医疗器械临床评估的全新指导文件MEDDEV 2.7/14版在欧盟**上正式发布。该指南明确了现有的一些要求,对于制造商如何进行一个健全、系统的临床评价,以及如何证明数据和结论的科学有效性有了明确的指导。这也给制造商带来了新的挑战。
该指南涉及93/42/EEC和90/385/EEC指令范围内的制造商和公告机构。
该指南包括:明确临床评估意图、对评估各步骤的详细指导、明确等同性评估的条件、指出不可用于证明符合欧洲指令的临床数据的具体案例、关于临床评估报告新的时间安排,对于评估人员资质的较低要求、以及此前版本指南不包括的其他具体细节。
公司从2017年年初开展临床评估业务以来,为国内近两百家医疗器械企业提供了临床评估报告编撰服务,其中包括很多国内**的大型医疗器械企业。四版欧盟临床评估指南的发布,的确给企业带来了不小的挑战,此文对主要变化进行了梳理。

关于MDR涵盖产品范围和分类规则:
医疗器械的分类继续以前的类别,根据风险等级分为四类:I,II a,II b,III。但是,分类规则从18增加到22.具体分类规则的条件和变化如下:
关于经济运营商的义务:
该法规在章2条的定义中提出了“经济运营者”的概念。经济运营者是指制造商,授权代表,进口商,分销商以及系统或手术袋的任何组合或消毒。投放市场的自然人或法人。也就是说,负责按照法规生产设备(包括组合或灭菌),销售和上市后操作的自然人或法人
Medical Device Regulation 2017/745/EU法规是什么?
SUNGO集团凭借**网络和队伍为**客户提供法规性服务,帮助企业*贸易壁垒,在医疗器械行业尤为专长。
这主要包括:欧盟CE认证(MDD/MDR)、欧盟授权代表、医疗器械欧盟注册、欧盟自由销售证书、FDA注册(FDA510K)、FDA验厂辅导,陪审和翻译、ISO9001/ISO13485,中国药监局注册证、GMP体系辅导和生产许可证等项目。
-/gbaaeee/-
http://sungoyuan.b2b168.com